
新闻动态
News Information

-
- 总局发布调整药品注册受理工作的公告
药品注册申请可采取电子申报、邮寄或现场提交的方式提交申报资料,同时提交纸质文本和电子文档。药品注册申请人将相关资料邮寄至国家食品药品监督管理总局药品审评中心(以下简称总局药审中心)。

-
- 治疗用生物制品最新注册分类
2017年10月23日,CFDA发布《药品注册管理办法(修订稿)》,同时附件《生物制品注册分类和申报资料要求(试行)》将治疗用生物制品进行了重新分类,由原来的15类变为5类,分类也更加明确。

-
- 重庆市工商联换届,唐德江董事长当选副主席
7月7日,重庆市工商联(总商会)第五次代表大会闭幕,会上选出了重庆市工商联主席(总商会会长),副主席(副会长),专职主席、兼职副主席、副会长在内的新一届市工商联领导班子。

-
- 桑国卫院士走进希尔安
7月25日,全国人大常委会原副委员长、中国工程院院士、中国药学会理事长桑国卫率调研组来渝调研并走进希尔安,听合川区副区长吴景明介绍了合川区医药产业发展情况,并参观了希尔安企业文化展示厅。
-
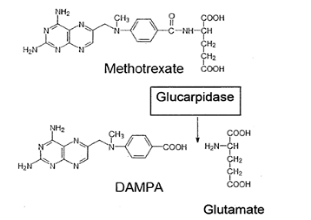
- 科润生物再出1类新药,可解肿瘤化疗引起的肾中毒
近期,公司自主研发的生物制品1类新药-“注射用重组羧肽酶G2”,目前已向重庆市食品药品监督管理局提交了新药临床申请,于4月中旬顺利完成现场核查工作。




